挑战与因应:TRIPS-plus背景下的药品专利链接制度
近年来,欧盟和美国为了继续保持国际优势竞争地位,利用TRIPS协定的弹性条款,通过区域贸易协定或者双边协定推行TRIPS-plus条款,药品专利链接制度就是美国的重要着力点之一。我国作为医药大国,创新能力不足,仿制药发展也参差不齐,建立药品专利链接制度既有现实需求,同时也面临较大挑战。以《中美第一阶段经贸协议》为切入点,以TRIPS-plus为基本背景,探讨药品专利链接制度建立的必要性,分析建立药品专利链接制度面临的挑战,最后从法律层面提出TRIPS-plus背景下建立药品专利链接制度因应之策。
TRIPS-plus;药品专利链接制度;挑战;因应
《与贸易有关的知识产权协定》(TRIPS协定)实施以来的近30年间,在减少国际贸易中的扭曲与阻力、提升知识产权保护水平等方面发挥了积极作用。然而,基于保持国际优势竞争地位和维护国家核心利益之战略考虑,发达国家提高知识产权全球保护水平的行动并未停止,继续谋求强化而不仅是维持TRIPS协议的现有义务。美东时间2020年1月15日,中美双方在美国华盛顿签署《中华人民共和国政府和美利坚合众国政府经济贸易协议》,在该协议的知识产权章节,就商业秘密和保密商务信息、药品相关的知识产权、专利、电子商务平台上的盗版与假冒、地理标志等知识产权问题进行了较为详细的规定。其中很多条款都超过了TRIPS协定对成员国设定的义务范围。这种超越TRIPS协议的相关规定、推行高标准知识产权保护水平的条款被学者们称为TRIPS-plus条款。从广义上说, TRIPS-plus条款是指旨在提高知识产权权利保护水平和扩展权利保护范围的、高于或者超出TRIPS协议最低保护标准的任何要求和条件,或者旨在缩减权利限制和例外的范围、削弱TRIPS协议弹性条款的措施。其来源主要有双边/区域自由贸易协定、知识产权协定、投资协定, 还包括在WIPO体制内缔结的新协定、WTO加入程序以及一些国家的国内法。美国作为世界医药知识产权强国,通过TRIPS-plus条款有利于充分实现本国医药产业的利益,其中,药品专利链接制度是其重要着力点之一。我国作为发展中国家,药品自主创新能力不足,研发能力较弱,直接承继对药品专利保护程度较高的药品专利链接制度显然不符合我国的国家利益,全盘拒绝固然可以避免对发达国家的药品专利进行高水平保护,但也错失了我国药品领域改革的良机。面对药品领域层出不穷的问题,给予知识产权低水平的保护固然可以一时保护我国的仿制药企业,却难以激发整个社会鼓励创造的内生动力,长此以往,将会扼杀企业的创造热情,不利于促进药品可及,维护公众健康。面对发达国家的步步紧逼和国内制药企业的现实问题,药品保护法律似乎陷入了两难的境地。为了拨散药品专利链接制度在我国建构的迷雾,有必要对TRIPS-plus背景下的药品专利链接制度进行进一步的研究。首先,探讨药品专利链接制度建立的必要性,其次,分析我国建立药品专利链接制度给我国带来的挑战,最后,提出我国建立药品专利链接制度的因应之策。
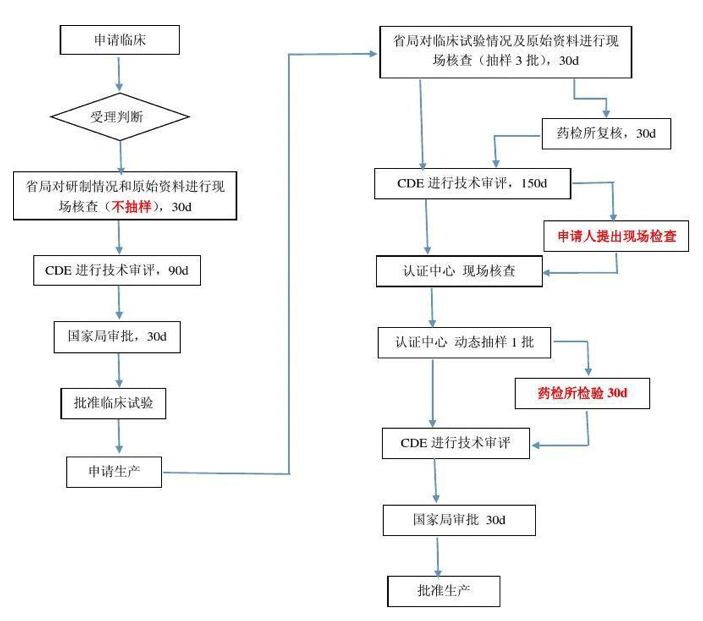
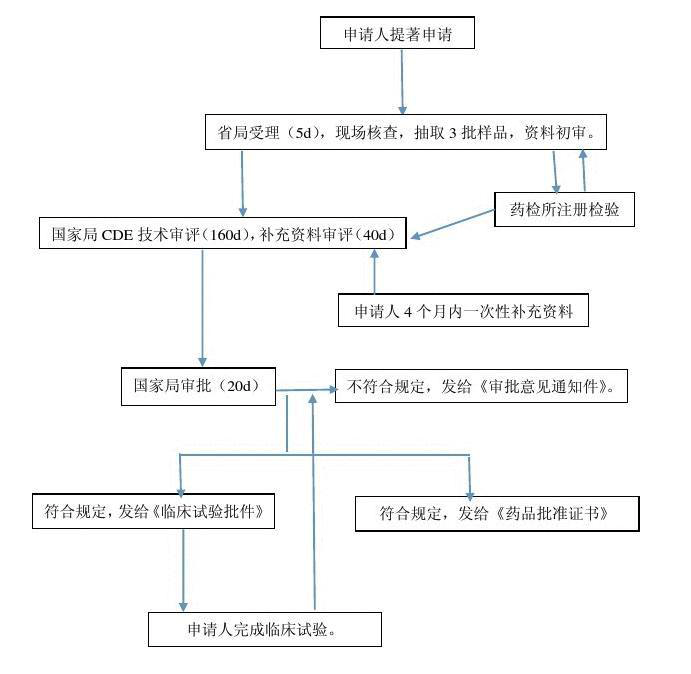
药品专利链接(patent linkage),是指仿制药上市批准与创新药专利期满相“链接”,即仿制药注册申请应当考虑已上市药品的专利状况,从而避免可能的专利侵权。药品专利链接制度是美国为维持其知识产权强国地位而着力推行的TRIPS-plus条款。探讨药品专利链接制度的挑战及因应之策,一个前提性问题是:在我国建立药品链接制度是否必要?透视国内和国外两个空间,分析内部和外部两个层面,探讨药品专利链接制度在TRIPS-plus背景下建立的必要性。美国凭借其在国际社会中强大的议价能力,将TRIPS-plus条款作为政策工具,通过以经济援助或科技合作作为交换及“301调查”等方式来推行其知识产权标准化战略。我国作为世界上最大的发展中国家,自2010年起,经济总量已跃居世界第二位,经过多年的发展,综合国力已不容小觑。由于长期存在的贸易不平衡,2018年,美国掀起了中美贸易争端。为了追求稳定的发展环境,扩大对外开放的深度、广度,坚持与美国打贸易战并不符合我国的国家利益。为了与美国达成协议,中国必然要在某些方面进行妥协。长期以来,对药品知识产权的保护一直是美国的重要诉求之一,药品专利链接制度作为美国保护药品知识产权的重要制度之一,更是美国在谈判中的必争之地。2020年,中美签订《中美第一阶段经贸协议》,药品专利链接制度部分内容的建立已成为我国的国家义务。因此,我国药品专利链接制度的建立面临巨大的外部压力,建立药品专利链接制度是促进我国产业升级、扩大对外开放的重要选项。TRIPS协定缔结之后,由于不满足于TRIPS协定的“最低保护标准原则”,在国内跨国企业利益集团的推动下,发达国家开始调整国际知识产权政策,通过TRIPS-plus条款来推行国内知识产权标准全球化战略。近年来,TRIPS-plus条款扩张的趋势日益明显:如,据美国贸易代表处官网资料显示,截至目前,美国已经签订了20个双边和多边自由贸易协定,如United States-Mexico-Canada Agreement、Singapore FTA、Bahrain Free Trade Agreement等。随着双边/多边自由贸易协定的不断签订,越来越多的国家将会被纳入协定的覆盖范围。积极参与制定自由贸易协定,有利于将我国的国家利益上升为国际规则,扩大国际影响力,不断增强我国在国际规则制定中的话语权。踱步在国际规则制定的门外,一旦形成惯例,再行进入,将愈发被动。一味拒绝签订自由贸易协定固然可以避免政策妥协,却也错失了参与制定全球规则的良机。药品是特殊的商品,药品法律的制定不仅关涉原研药企业和仿制药企业的利益,更与公众健康息息相关。根据我国药品管理法的相关规定,药品上市需要证明药品的安全性、有效性和质量可控性。符合仿制药审评审批的条件,药品即可上市。然而,允许药品上市并不意味着排除了药品上市的侵权风险。专利权是独占实施权,在原研药的研发过程中,为了占领市场,垄断利益,原研药企业往往会提前进行专利布局。若仿制药上市销售,可能会侵犯原研药企业的专利权。进而,不但原研药企业的利益因侵权而受损,仿制药企业也将承担高额的损害赔偿责任。专利声明制度是药品专利链接制度的重要内容之一,仿制药申请人在进行上市申请时,应当提交药品专利状态的说明,从而避免潜在的侵权风险。 也就是说,在核准仿制药上市的程序中必须额外考虑原研药的专利是否存在及其有效性。若仿制药上市将侵害原研药的药品专利,即不予上市许可; 反之,若仿制药上市不侵害他人专利权,即会发给上市许可。药物研发高投入、高风险、高收益,且周期非常长。基于2016年“制药基准测试论坛”给出的数据来看,从目标产物的确认到首次批准上市的时间平均需要13.8年。而对于发明专利,我国只给予了其20年的专利保护期,在专利保护期内甚至难以收回研发成本。面对如此严峻的研发态势,企业研发创新药动力不足。药品专利链接制度则给创新药的研发打了一针强心剂。第一,Hatch-Waxman 法案规定了新药申请者可获得专利延长期,补偿其在临床试验和药品审评中所消耗的时间。第二,创新药的药品试验数据独占保护。在 Hatch-Waxman 法案中,对不同类型的药品规定了不同的药品数据独占时间,如对含有新化学实体的新药,给予 5 年的数据独占保护。诚然,我国制药产业创新能力弱,坚持引进药品专利链接制度可能会给我国本不发达的原研药产业带来灭顶之灾,但也应清醒的认识到,制度本无高下之分,如何应用制度才是关键。因此,如何借鉴药品专利链接制度,调适我国药品法律制度,才是解决问题的不二法门。诚如上文所述,药品法律制度关乎公众健康,而药品价格是制约药品可及和公众健康问题的关键。由于原研药高投入、高风险、高收益,且周期非常长,为了收回研发成本,原研药的价格常常十分高昂。而仿制药由于研发成本较低,药品价格也较低,有利于促进药品可及,维护公众健康。确立药品专利链接制度有利于助推仿制药的发展:第一,仿制药简化申请制度有利于加快低成本仿制药的上市;第二,监管审批机构链接制度有力于加强药品上市审评审批机构与专利审查机构的职能链接,减少可能的专利侵权;第三,首仿药市场独占期制度有利于鼓励仿制药企业挑战新药专利,获得市场独占期。我国作为仿制药大国,药品专利链接制度为促进我国仿制药的发展提供了又一契机。目前,我国多部门对药品专利链接制度的建立提出了指导性意见。2017年5月,食品药品监管总局就鼓励药品医疗器械创新保护创新者权益征求意见,提出建立药品专利链接制度;2017年10月,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,提出探索建立药品专利链接制度;2019年11月,中共中央办公厅、国务院办公厅印发《关于强化知识产权保护的意见》,指出探索建立药品专利链接制度、药品专利期限补偿制度;2020年9月,国家药监局发布了《药品专利纠纷早期解决机制实施办法(征求意见稿)》,形成了具有中国特色的药品专利链接制度的框架;2020年10月,第十三届全国人大常委会对专利法进行了修改,将药品专利链接制度正式引入我国立法之中。综合国内、国际环境,药品专利链接制度的建立已形成了广泛共识。 建立药品专利链接制度不仅承载了我国履行双边条约义务、参与全球规则制定的多重考虑,更是我国前端解决侵权纠纷、助力药品研发创新、切实维护公众健康的现实需求,在我国建立药品专利链接制度已形成广泛共识的基础上,应当直面挑战,深入研究制度引入的社会环境差异,分析药品专利链接制度与我国现行法律规定的不兼容之处,在引入与调试之间找出中国特色的解决之道。在美国,药品专利链接制度的产生经历了三个阶段。1962年以前,粗放而野蛮。仿制药企业在原研药专利过期之后提交证明仿制药安全性的资料即可上市。1962年-1983年,仿制药审批低迷,药品上市要经过有效性和安全性双重检验。市场上绝大部分药品是原研药。1984年以后,药品法律制度愈加完善,原研药和仿制药良性发展。在美国,药品专利链接制度实施的产业环境是原研药企业研发动力高,研发能力强,医药市场以实力强劲的原研药企业为主。确立药品专利链接制度,不仅解决了其仿制药企业发展低迷的现状,更通过药品试验数据独占保护期制度、专利期延长制度等促进了原研药产业的发展。而对于中国医药市场而言,其呈现出来与美国完全相反的形态,我国缺乏强大的原研药企业,创新实力薄弱,市场以仿制药为主,但仿制药企业的水平也良莠不齐,行业中存在着重复仿制、低水平仿制等固有问题。不仅仿制药发展水平不足,原研药研发能力也很低,且以仿制药为主。若我国借鉴药品专利链接制度,对于我国原研药企业来讲,相较于国外发达国家,我国原研药企业研发能力较弱,在我国医药市场占比也较低。一旦给予研发创新药法律、政策上的重大利好,不仅会激励本国企业进行创新药的研发,更会激励国外发达国家的企业积极进行创新药的研发、专利申请、上市,将会进一步挤占我国发展能力本就不足的原研药企业的市场空间。对于我国仿制药企业而言,美国是在原研药企业发展强劲的基础上通过实施药品专利链接制度促进了仿制药的发展,而我国是在创新药发展不足的情况下实施药品专利链接制度,该制度能否促进仿制药企业发展不无疑问。另外,原研药是仿制药的源头活水,原研药发展不足,仿制药将面临无药可仿的局面,在药品研发能力不足的情况下,强行通过制度设计揠苗助长难免不会出现适得其反的情况。目前,我国现行法律法规中已经出现了药品专利链接制度的雏形。建立药品专利链接制度,不仅要与药品专利链接制度的现行规定相协调,还涉及专利法、药品管理法、行政诉讼法等的协调,以及专利审查机构、药品上市审评审批机构、法院之间的协调。修订药品保护法律,牵一发而动全身。在传统上,专利法和药品管理法具有不同的政策考虑和立法目标。专利审查机构依据专利法相关的法律法规审查是否符合专利授予条件,药品上市审评审批机构依据药品管理法、药品注册管理办法等审查药品是否符合上市条件,二者相互独立。鉴于药品对公众健康的重要作用,国家对药品上市设定了严格的申请条件和流程。如下图所示。而在药品专利链接制度之下,药品审评审批机构需要与专利审查机构职能链接,这样一来,将会使本就复杂的药品审评审批程序变得更加复杂,而且需要配备更多的人力和物力资源,增加大量行政成本。
我国与美国属于不同的法系,美国是英美法系,崇尚法律的实用性,而我国是大陆法系,成文法是我国法律的重要特征。因而,在借鉴他国法律时,要特别重视法律的兼容性,也就是说,在法律体系内部,不能出现自相矛盾的情形。若在我国确立药品专利链接制度,将给我国法律体系的融贯性带来挑战。第一,药品专利链接制度中拟制侵权的规定与我国专利法的基本理念存在冲突。拟制侵权是指在药品专利链接中,药品专利权人针对仿制药商提起上述第4类专利挑战声明所引发的专利侵权诉讼。也就是说,美国将提起第四类专利声明的仿制药上市审批申请的行为“视为侵权”。而依据我国专利法的规定,专利权是独占实施权,仿制药申请上市审批并未侵犯专利权人的专利权,而且,根据我国专利法的规定,即使侵犯了专利权人的独占实施权,如果是为提供行政审批需要的信息,也不视为侵权。第二,药品专利链接制度中专利挑战制度与我国现有民事诉讼体系存在冲突。在药品专利链接制度下,若仿制药企业发起专利挑战,原研药企业提起诉讼,FDA将根据法院对专利侵权诉讼的审理结果视情况决定是否授予专利权。而在我国,若被告在专利侵权诉讼中提起涉案专利无效,法院无权判断专利的有效性,须待专利复审委员会就专利的有效性做出裁决后才能继续审理。目前,移植美国药品专利链接制度在我国面临较大的挑战,一方面,我国与美国实施该制度的产业环境、发展状况并不相同,另一方面,我国移植该制度的立法成本也较高。在我国建立药品专利链接制度形成广泛共识的情形下,该挑战能否构成我国难以建立药品专利链接制度的制度性障碍,一个前提性的问题是,上述挑战是否是不可避免且难以克服的。第一,就立法环境而言,尽管我国与美国并不相同,但我国药品行业也出现了同美国类似的问题,具有借鉴的可能性,况且,借鉴并非全盘接受,可以结合我国的产业情况、发展水平,有选择的继受并调适,对于超出我国药品产业发展水平的,大可不必在现阶段设定法律。第二,就立法成本而言。一方面,拟制侵权本身就是制度的例外,与我国现行法律相悖也在情理之中,另一方面,在我国,如何协调专利侵权诉讼与专利复审委员会对专利有效性判断二者之间的关系,从而促进效率的提升是学术界和实务界研究的热点话题,我国现行处理方式的弊病已经凸显,将药品专利链接制度作为立法的重要考量,也有利于法律的完善。第三,组成药品专利链接制度的系列制度共同作用,相互协调,使得该制度的效用得到最大发挥。药品专利链接制度不是单一的制度,而是由众多子制度组成的“制度群”。在该制度群中,不同的制度发挥不同的作用,如,有的制度主要作用在于促进仿制药的发展,却不利于原研药的发展,而有的制度主要作用在于促进原研药的发展,却不利于仿制药的发展,单独施行某一制度可能会带来很大的弊端,但是,如若共同施行,相互配合,互融互通,可以使得该制度的弊端降到最低,从而使得该制度的效用得到最大发挥。因此,我国完全有理由借鉴美国药品专利链接制度,并结合我国国情,建立中国特色的药品专利链接制度。近年来,由于国际社会结构的平行与分散、贸易保护主义的抬头等原因,TRIPS-plus条款的数量不断攀升,全球知识产权保护水平也不断提高。以美国和欧盟为首的欧美发达国家通过自由贸易协定或签订双边条约等的方式推行高标准的知识产权保护制度。随着谈判的国家(或地区)越来越多,将有更多的国家(或地区)被纳入确立药品专利链接制度的国家范围之中,高标准的知识产权保护制度将被逐步确立。而共识一旦确立,我国再加入自由贸易协定或签订双边条约时的议价能力将会大大降低。因此,我国应积极参与规则制定,发出中国声音。第一,积极参与多变条约的制定。作为最大的发展中国家,我国有责任积极参与到国际规则制定中去。在规则制定早期,发表关键意见,深化交流与合作,争取在国际知识产权谈判中的话语权。第二,积极参与双边条约的制定。和平稳定的社会环境是经济发展的前提,在对方并未触及谈判底线的情形下积极磋商。就药品专利链接制度而言,可以将其中的具体制度分为三类:绝对不能接受的制度,对我国利大于弊的制度,视情况可以接受的制度。根据不同的情形选择谈判策略。第三,在谈判过程中,将我国优势知识产权作为谈判砝码,掌握主动权。我国是发展中国家,药品研发能力不足,医药行业仍以仿制药为主。因此,药品法律制度的设计应着重促进仿制药的发展。在借鉴药品专利链接制度时,也应当以此为基本导向。药品专利链接制度由若干具体的制度组成,如橘皮书制度,专利声明制度,拟制侵权制度,药品试验数据独占保护期制度,仿制药简化申请制度,首仿药独占保护期制度,专利期延长制度等。在这些制度中,有些制度有利于促进仿制药的发展,有些侧重于促进原研药的发展,有些则是辅助性的制度。有些制度与我国现行法律法规没有冲突,有些制度则与我国现行的法律法规存在不兼容之处。有些制度是我国在双边条约中承担的国际义务,有些制度则属于我国自由选择的范围。对于那些有利于促进仿制药发展且可能与我国现行法律法规兼容的,可以在调适后借鉴,如首仿药独占保护期制度、仿制药简化申请制度等;对于那些有利于创新药发展的制度,可以采取缩小保护范围、具体分类等方法使之适合我国发展情况后借鉴,或采取渐进式立法,或暂时不予立法,如药品专利延长保护期制度,等。在药品专利链接制度立法过程中,可以结合我国实际情况,对不同的制度进行分类,分情况立法。尽管我国经济总量很大,但行政水平、司法现状、创新能力和欧美发达国家相比仍有较大差距。第一,就行政水平而言,药品专利链接制度的重要内容是药品审评审批机构与专利审查机构的职能链接,而我国,虽不断推动政府简政放权,建设服务型政府,但与发达国家相比,仍有较大差距。就司法现状而言,在药品专利链接制度中,若专利权人想法院提起诉讼,法院需解决专利侵权问题,而专利侵权案件往往涉及专业问题,与技术相关,非专业人士难以判断。因而,在涉及专利有效性判断时,往往交由专利复审委员会解决。就创新能力而言,药品专利链接制度不仅解决了仿制药发展低迷的状况,还进一步刺激了原研药的发展,而在我国,原研药发展水平低,研发能力不足,借鉴不当可能会反而给发达国家的原研药企业做了嫁衣。因此,在我国行政水平、司法现状、创新能力等并未达到移植该制度的基本条件的情况下,对于该制度,可以采取分阶段立法的方式,根据每一阶段的发展水平谨慎立法。在我国确立药品专利链接制度,不仅是我国履行双边条约义务、参与全球规则制定的需要,也是前端解决侵权纠纷、助力药品研发创新、切实维护公众健康的需要,在我国已建立了药品专利链接制度的雏形且多部门发文主张建立药品专利链接制度的情形下,药品专利链接制度的建立在我国已形成了广泛共识。然而,在我国建立药品专利链接制度仍面临较大的挑战,我国的基本国情和美国存在较大差异,同时立法成本也比较高。然而,该种挑战并非是不可避免且难以克服的,从长远来看,也是我国药品保护法律制度回应现实、面向未来的务实之举。鉴于此,我国应积极参与国际规则制定,发出中国声音,并采取分情况立法、分阶段立法的方式使之在契合我国基本国情的基础上成为中国特色的药品专利链接制度。
[1] 吴焕焕. TRIPS-plus协定扩张的理论研究[D].华东政法大学,2018.[2]杨静,朱雪忠.中国自由贸易协定知识产权范本建设研究——以应对TRIPS-plus扩张为视角[J].现代法学,2013,35(02):149-160.[3]肖建玉,沈爱玲.构建符合我国国情的药品专利链接制度[J].现代中药研究与实践,2010,24(05):83-85.[4]刘颖.后TRIPS时代国际知识产权法律制度的“碎片化”[J].学术研究,2019(07):53-63+2.[5]张正怡.TRIPs-plus条款对我国知识产权政策的启示[J].法治论丛,2010,25(05):62-69.[6] 杨静.美国自由贸易协定中TRIPS-plus规则的立法动力分析[J].知识产权,2011(07):86-90[7]丁锦希,韩蓓蓓.中美药品专利链接制度比较研究[J].中国医药工业杂志,2008,39(12):950-955.[8]陈敬,史录文.美国药品专利链接制度研究[J].中国新药杂志,2012,21(22):2591-2594+2599.[9]李红团.构建合乎国情的药品专利链接制度[J].中国新药杂志,2018,27(17):1953-1963.[10]李蓓.中美药品专利链接制度研究[J].科技与法律,2018(01):10-18.[11]李想.医药专利链接制度运行机理研究[J].电子知识产权,2019(03):13-21.[12]梁志文.药品专利链接制度的移植与创制[J].政治与法律,2017(08):104-114.[13]袁锋.我国移植和构建专利链接制度的正当性研究——对现行主流观点之质疑[J].科技与法律,2019(06):1-12.[14]郑淑凤.专利链接中拟制侵权的理论基础与实施问题[J].电子知识产权,2019(12):83-94.[15] Sisule Musungu, Graham Dutfield.Multilateral A-greements and a TRIPS-plus World: The World IntellectualProperty Organization[R]. Geneva:QUNO/Geneva andQUIAP/Ottawa,[16] Ron A.Bouchard et.al,Empirical Analysis of Drug Approval-Drug Patenting Linkage for High Value Pharmaceuticals,8 NW.J.Tech.&Intell.Prop.174,177 (2010)



